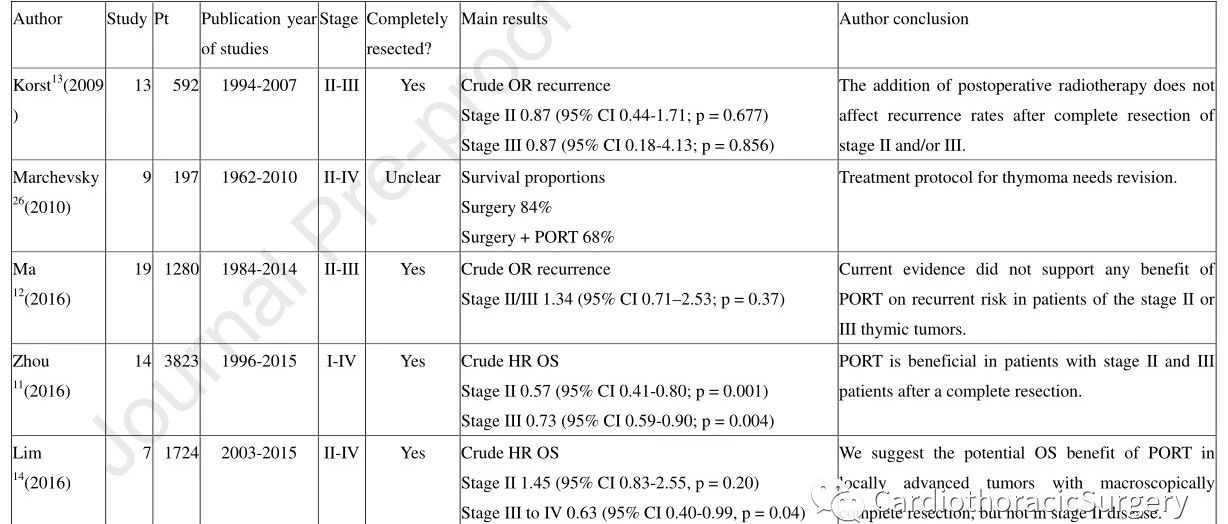
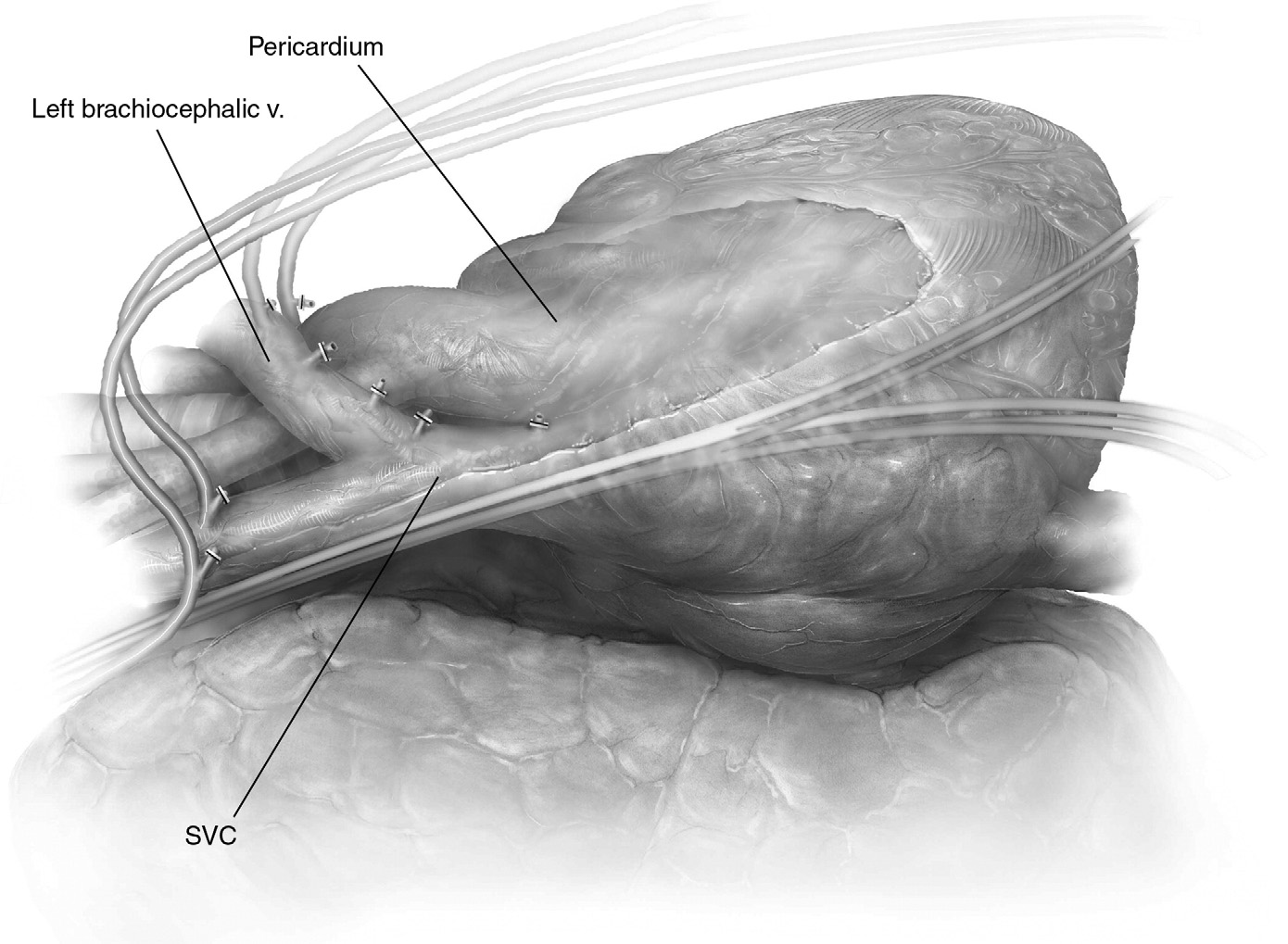
1. 胸腺恶性肿瘤是否应接受淋巴结切除术?
众所周知,手术切除是胸腺恶性肿瘤的标准治疗手段。然而,对于恶性胸腺肿瘤淋巴结转移和术中淋巴结清扫的预后意义仍不清楚。鉴于此,来自韩国的Yoohwa Hwang等开展了一项研究,旨在确定胸腺恶性肿瘤淋巴结转移的预后意义以及淋巴结清扫术(LND)的作用。文章发表在近期的JTO杂志上。
研究者纳入2000年至2013年间,1,597例因胸腺恶性肿瘤接受胸腺切除术的患者资料。研究者评估淋巴结转移的预测因素和LND的预后意义。并将患者分为两组:1)LND +组,接受意向性LND(446例,27.9%); 2)LND-组,未接受意向性LND(1,151例,72.1%)。两组患者进行倾向性匹配分析。
该研究发现,298例胸腺瘤患者中有20例(6.7%)发现淋巴结转移,148例胸腺癌患者中有47例(31.7%)发现淋巴结转移。在多变量分析中,胸腺癌(HR:19.2,p <0.001)和肿瘤大小(HR:1.09,p = 0.02)是淋巴结转移的重要预测因素。pN1和pN2的10年无复发率(FFR)明显低于pN0(p <0.001)。LND没有增加手术死亡率或并发症。LND +和LND-组10年FFR率无显著差异(胸腺瘤为82.4% vs 80.9%,p= 0.46; 胸腺癌为45.7% vs 44.0%,p=0.42)。
所以研究者认为淋巴结转移是胸腺恶性肿瘤的重要预后因素。虽然LND没有改善胸腺恶性肿瘤的长期预后,但LND在准确分期和改善预后预测方面发挥了重要作用。
原文题目:Impact of Lymph Node Dissection on Thymic Malignancies: Multi-Institutional Propensity Score Matched Analysis
2. 胸腺瘤术中需行淋巴结采样
外科手术是治疗胸腺瘤的最佳措施,但术中是否需行淋巴结采样尚不清楚。此外,胸腺瘤淋巴结转移对预后的影响亦不清楚。针对上述问题,来自田纳西大学健康科学中心胸外科的 Benny Weksler 等利用 SEER 数据库中的资料,对接受胸腺瘤切除且作了淋巴结病检的患者进行分析,其研究结果最近发表在 The Journal of Thoracic and Cardiovascular Surgery 上。
研究者从数据库中筛选出 442 例接受手术治疗的的胸腺瘤患者,每例患者至少接受了 1枚淋巴结的评估,采样淋巴结的中位数是 2 枚,其中 59 例患者(13.3%)至少存在一枚淋巴结转移,且有淋巴结转移的患者年龄及肿瘤大小均小于淋巴结阴性的患者。
淋巴结阳性患者的中位生存期为 98 个月,而淋巴结阴性患者的中位生存期为 144 月。多因素分析显示淋巴结转移是预后不良的独立危险因素。80% 的淋巴结阳性患者分期被提高,多数由 Masaoka-Koga III 期变为 IV期。
总之,淋巴结转移情况是胸腺瘤患者重要的预后因子,在对淋巴结转移的认识更加明确之前,胸腺瘤切除术中有必要行区域淋巴结采样。
3. 第八版胸腺瘤分期评述

Enrico Ruffini教授
迄今为止,外科手术是治疗胸腺肿瘤的基本手段。在ITMIG领导下通过与区域和社会为基础的兴趣小组合作(ESTS,JART)协作,随着新的胸外科技术的发展,众多关于胸腺手术的历史教条受到了质疑和挑战。因此来自意大利的Enrico Ruffini教授等通过文献回顾,提出目前胸腺肿瘤治疗的外科治疗进展,文章发表在近期的Lung Cancer杂志上。主要为以下四点:
1. 包括电视辅助胸腔手术(VATS)和机器人辅助胸腔手术(RATS)在内的微创技术(MIT)是早期胸腺肿瘤的标准治疗手段。麻省理工学院的研究证实MIT在术后并发症,局部复发率和生存率方面并不逊色于开放手段。麻省理工学院的研究同时表明MIT在术后住院时间,术中出血量,美容效果方面均优于开放手术。
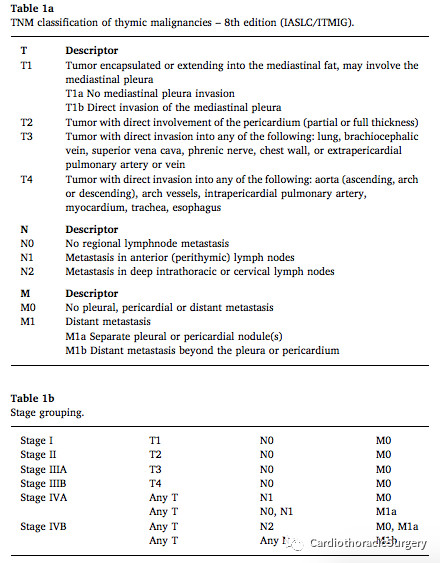
2. 胸腺肿瘤采用ITMIG/IASLC TNM分期系统,这就需要胸外科手术中根据IASLC/ITMIG淋巴结图谱进行模式转变,包括区域淋巴结的手术管理。
3. 有学者提出局限性胸腺切除术的概念,即对于非重症肌无力的I-II期肿瘤患者不接受全胸腺切除术,但目前的结果并不一致。所以,在更成熟的数据发布之前,除了胸腺切除外,一定要遵守现行指南推荐的全胸腺切除术。
4. 对于胸膜受累的局部晚期IVa期患者,予以胸膜切除术包括胸膜切除术/剥脱术或胸膜外全肺切除术完全切除病灶,并采用多学科治疗模式,通常具有良好的长期结果。
简单的说,微创手术、淋巴结切除、全胸腺切除(即使是早期胸腺瘤)、胸膜切除(胸膜受累的局部晚期IVa期),这些新概念和技术值得每一位胸外科医生重视。这些治疗策略可以改善胸腺肿瘤患者的预后。
原文题目:Optimal surgical approach to thymic malignancies: New trends challenging old dogmas.
4. 第八版胸腺瘤分期评述
胸腺肿瘤往往与自身免疫综合症相关,这引起了临床医生对其的好奇。胸腔播散是胸腺肿瘤独特的生物学行为,且存在组织学异质性。由于胸腺肿瘤相对罕见,因此很难对这类肿瘤的组织学分型和分期达成共识。
近年来,许多研究者提出不同的胸腺肿瘤分期标准,但是大多数并未获得认可。过去40年,至少提出了14种不同的分期标准。
3-4年前,Masaoka及其同事首次提出了胸腺瘤的分期系统。虽然,该分期系统只是基于93例患者进行分析,但该系统经过时间的考验证实可以很好的预测患者的预后,由此得名的Masaoka分期系统仍然是今天使用最广泛的分期标准。随后很多研究者尝试予以改良,其中最有名的是1994年Koga及其同事提出的修订方案。
然而,依然存在问题,有些问题来源于临床及病理描述。例如,什么是“肉眼侵犯邻近器官”?如何才能确定肿瘤''严重粘连而不是穿透纵隔胸膜''?纵隔胸膜在标本的哪个部位?该分类是否适用于胸腺癌,还是只针对胸腺瘤?这些条目由Detterbeck及其同事逐项列出, 并着眼于修改分期系统。
为了促进对该类罕见肿瘤的研究成立了国际胸腺恶性肿瘤兴趣小组(ITMIG)。ITMIG的一个主要目标提出以证据为基础的新的TNM分期,该项目由AJCC发起。作为国际肺癌研究协会的合作伙伴,ITMIG组建了15个国家50个研究机构的6000例患者的全球数据库。
根据这些数据研究者基于肿瘤大小,淋巴结和转移成立了新的分期系统。该分期系统表明T分期具有重大意义,因为淋巴结及远处转移较为少见,根据肿瘤的浸润深度分为纵隔脂肪(T1a),纵隔胸膜(T1b),心包(T2)和其他邻近器官(T3,T4) 。
需要重点提的是,T分期的描述是基于显微镜下表现和病理评估其侵犯情况,而不是''宏观侵犯’’。目前,纵隔胸膜和心包予以单独描述,这有助于将来更为彻底的评估其预后意义。邻近器官的侵犯基本上可分为“可切除”(T3)和“不可切除”(T4)两类。
尽管病例数较多,可用于淋巴结及远处转移统计的例数仍然不多,未发现统计学显著差异。因此,建议将来采集N和M数据时更加系统化。目前, N的描述主要是基于淋巴结的分布(N1 胸腺前/周围,N2 胸内/颈部),并提供解剖学边界。M的描述区分胸膜和心包结节(M1a)和远处转移包括肺内转移(M1b)。随着定义的明确,将来有助于进一步分析。
值得注意的是,将来需要建立一个包括胸腺癌和胸腺类癌在内的所有胸腺恶性肿瘤的统一分期系统。这不仅需要大样本量还需要严谨的统计学家参与。将来需要分析不同切除状态患者的预后和复发模式,不仅是接受R0切除的患者。
然而,由于目前的分析结果主要是基于收集的回顾性数据,依然存在很多问题。纵隔胸膜侵犯(T1b期),T4侵犯到主动脉或心肌,是否真的得到了病理证实?能否准确界定淋巴结状态,当前大多数外科医生在切除胸腺时一般不会进行系统淋巴结清扫。对于胸腺肿瘤怎么样才算是完整淋巴结清扫?
附:胸腺瘤第八版TNM分期
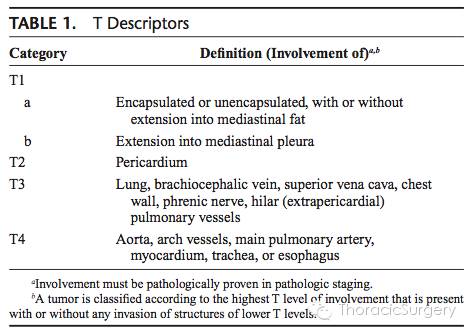
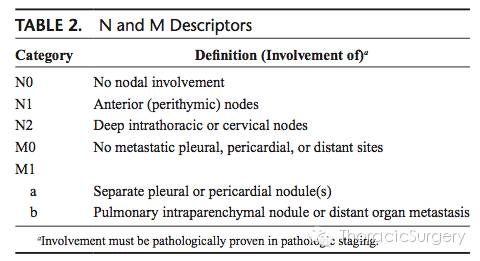
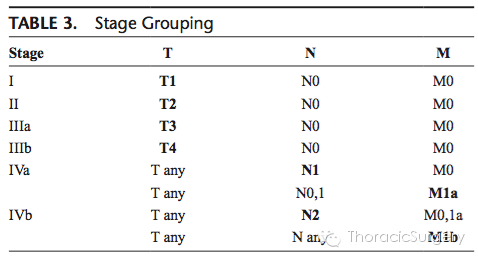
原文题目:The IASLC/ITMIG Thymic Epithelial Tumors Staging Project: Proposal for an Evidence-Based Stage Classification System for the Forthcoming (8th) Edition of the TNM Classification of Malignant Tumors
原文链接:http://www.xxwk.net/archives/1819