编译:广东省人民医院 广东省肺癌研究所 王梦敏 张潮 钟文昭 杨学宁
ICAN研究PI:吴一龙教授

ICAN研究是由广东省人民医院广东省肺癌研究所吴一龙教授牵头的一项全国多中心非干预性研究,此研究主要探索中国手术完全切除的肺腺癌患者EGFR突变状态,临床结局以及复发危险因素等之间的相关性,初步研究成果于ESMO大会进行报道。此次为历时长达9年随访后最终分析结果发表于JTOCRR。

研究设计:
本研究扩展期对前期收集早期肺腺癌术后患者进行长达9年随访,首要研究终点主要是EGFR 突变状态以OS,次要研究终点是DFS,复发时长以及影响预后因素等,对术后辅助化疗在不同EGFR突变状态患者中进行基于预后相关事后分析。最终,共有472例I-III期中国肺腺癌患者被纳入分析,其中I期273(57.8%)例,II-III期199(42.2%)例。
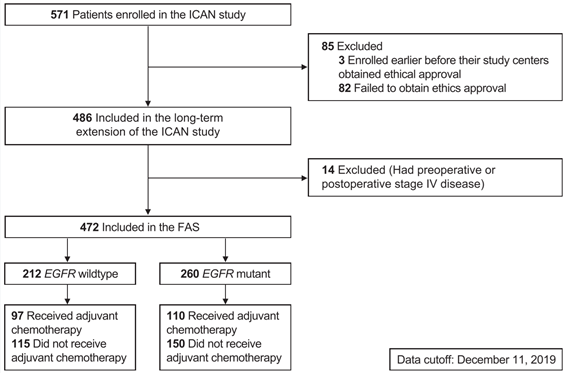
研究主要结果:
1. 患者基线特征
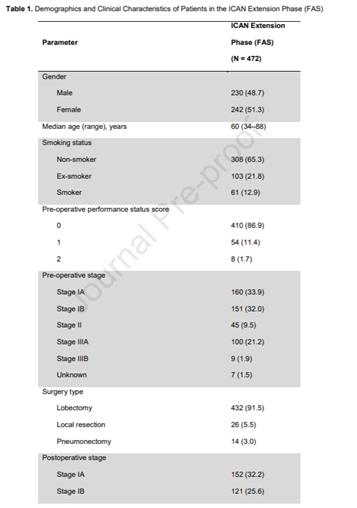
本研究拓展期患者人群以及临床特征均与初步研究结果相似。
患者平均年龄为60(34-88)岁,且近乎一半为男性 (230 [48.7%])。432(91.5%)例行肺叶切除术。
EGFR突变阳性260(55.1%)例,其中 Ex19 (121 [46.5%]) 缺失以及Ex21 L858R (122[46.9%]) 突变最为常见,且有4例(1.5%)患者为共突变。而Ex 18 G719X和Ex 20插入突变较为罕见,T790M突变仅13(5%)例。
本研究中EGFR突变状态与既往研究分布特征相似。
IA期、IB期、II期以及IIIA期EGFR突变阳性患者占比分别为63.2%、55.4%、54.1%、48.5%;6例IIIB期患者均为EGFR阴性。术后共有207例患者接受辅助化疗,其中97(46.9%)例为EGFR阴性,55(26.6%)例为EGFR Ex19 缺失,50(24.2%)例为Ex21 L858R突变,罕见突变仅5(2.4%)例。

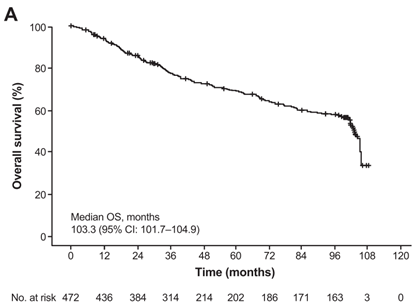
2. OS和DFS结果
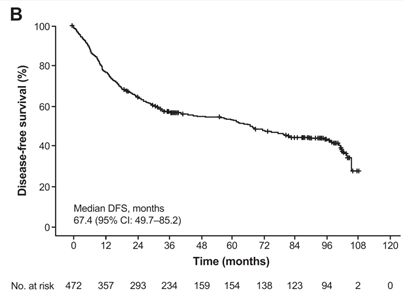
中位总体生存时间(mOS)为103.3个月且472位患者中有179(37.9%)位患者发生终点事件,而中位无病生存时间(mDFS)为67.4个月。其中,1-,2-,3-,5-,8-年累积OS率分别为93.8% (95% CI: 91.6–96.0), 85.8% (95%CI: 82.6–88.9), 77.2% (95% CI: 73.3–81.1), 68.9% (95% CI: 64.3–73.6), and 57.5%(95% CI: 52.2–62.8),而累积DFS率分别为77.1%(95% CI: 73.3–81.0), 64.7% (95% CI: 60.4–69.1), 56.6% (95% CI: 52.0–61.1),52.9% (95% CI: 48.2–57.7), and 42.8% (95% CI: 37.7–47.9)。
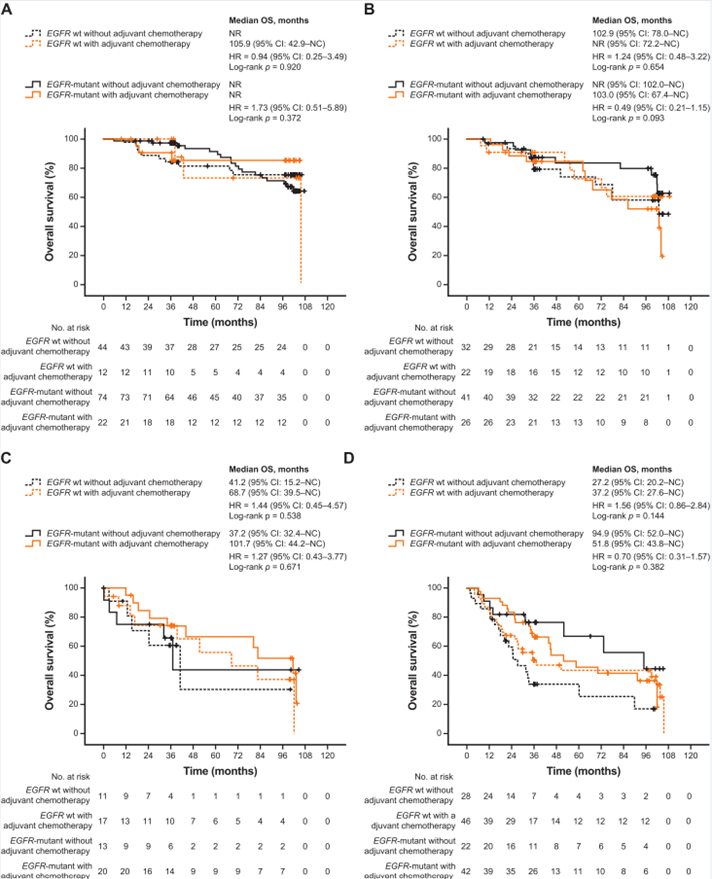
3. 基于预后相关事后亚组分析
本研究初步结果认为EGFR突变阳性患者3y-DFS较阴性患者明显提高(65.6% vs 56.8%, p = 0.0347),但拓展期研究结果却显示不论EGFR突变状态如何,所有术后患者之间mDFS无明显差异。
亚组分析显示术后未接受辅助化疗的患者mDFS (98.2 vs 27.2m, HR= 0.51 [95% CI: 0.40–0.65], P < .001)以及mOS (未达到终点vs 101.5 months, HR = 0.66 [95%CI: 0.49–0.88], p = 0.005)显著高于术后接受辅助治疗患者;将两组患者人口特征以及临床病理学特征进行比较,可知肺癌分期是辅助化疗指征的潜在混杂因素。与III期患者相比,IA、IB、II期患者校正后的OR分别为0.14(95%CI:0.08-0.25)、0.35 (95%CI:0.20-0.60)和0.96 (95%CI:0.49-1.86)。在调整分期后,无论患者术后是否接受辅助化疗,其mDFS以及mOS均无明显差异。
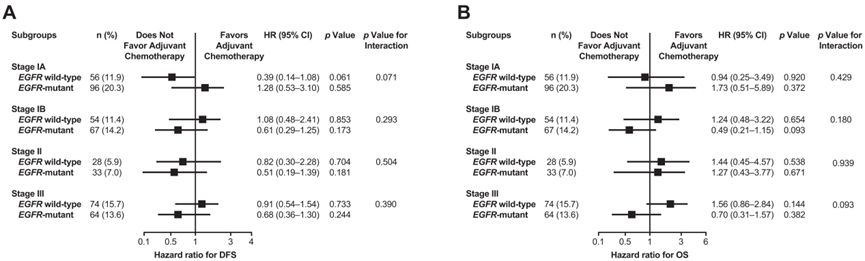
在术后各病理分期,不论EGFR突变状态如何,接受和未接受辅助化疗患者之间DFS和OS无明显差异。但携带EGFR突变IB-III期患者在接受术后辅助化疗后,其DFS时间似乎更短,且OS在IB或III期患者中获益较小。具有罕见EGFR突变I期肺腺癌患者似乎生存时间更短,仅有8例,仍需进一步研究。此外,除了EGFR突变III期未接受术后辅助化疗患者OS获益外,EGFR突变状态对患者DFS和OS没有显著影响。
3. 预后影响因素
通过共线性诊断揭示辅助化疗与其他预后之间的共线性,进一步因子分析并进行因子矩阵旋转发现四个独立预后因素,即吸烟(load: 0.905)、术后分期(load: 0.867) 和辅助化疗(load: 0.736),年龄(load: 0.958) 以及EGFR突变状态(load: 0.982)。
讨论:
在早期可手术肺腺癌中,携带EGFR基因突变的人群广受肿瘤学家的关注。对于该人群,辅助靶向治疗的疗效、辅助化疗的地位以及如何优选亚群和优化方案是目前讨论热点。近期,有关此问题的多项国际和国内研究发表,让我们对于以上问题有了更为深入的认识。我们在此综合进行讨论。
一、早期可手术肺腺癌EGFR突变状态和生存情况。 ICAN研究是一项肺腺癌完全切除术后全国多中心真实世界前瞻性非干预性研究。研究的目的是调查这些患者的EGFR突变状态、临床结局和复发风险因素。 ICAN研究显示,中国肺腺癌可手术患者EGFR突变率高,达到55.1%,最常见的突变类型是外显子19缺失和外显子21 L858R突变。不同病理分期的EGFR突变率没有差别。EGFR 突变是OS的重要独立预测因子。均与既往的报道的晚期肺腺癌相似。 ICAN研究显示,可手术肺腺癌术后随访期间的复发和死亡率高。术后5年的复发率达到50%,死亡率30%。提示仍然需要有效的辅助治疗降低复发,提高生存。 二、肺腺癌完全切除术后辅助化疗的地位 在ICAN研究入组的2010年,非小细胞肺癌的辅助化疗,是针对完全性切除术后的Ⅱ期和Ⅲ期患者的标准治疗。多个III期随机对照临床试验和meta分析证实术后辅助化疗能够使5年生存率提高5%,尤其对于Ⅲ期患者提高17%。彼时EGFR-TKI价格昂贵,且在辅助治疗中的证据不足。所以入组ICAN研究的大多数II/III期患者接受了辅助化疗。207例(43.9%)接受了辅助化疗,II/III期62.8%(125/199),I期30%(82/273)接受化疗,甚至IA期也有22.3%(34/152)接受化疗。 然而, ICAN的亚组分析显示,无论术后各分期EGFR突变状态如何,辅助化疗的生存结果都没有显着差异。也就是说,在真实世界中辅助化疗并没有使患者获益! 在国际多中心EGFR阳性肺腺癌辅助治疗研究ADARUA研究研究中,无论接受是否接受辅助化疗,各分期的辅助奥希替尼组DFS相似,即增加辅助化疗,可能在辅助奥希替尼基础上并无助益,起不到1+1>1的效果。不过,ADAURA研究亦未显示辅助化疗会导致预后受损。 为什么会出现这样的情况?在ICAN研究中我们未能找出确切的原因,但考虑有以下可能的原因:
-
完全切除术后的肺腺癌辅助化疗本身益处较小,在临床试验中,因为控制了严格的入组条件和方案实施,所以能够体现出差异,但在真实世界中,因为方案执行的强度和患者的全身情况等因素,最终抵销了辅助化疗的益处。 -
在接受辅助靶向治疗的患者中,与辅助化疗的获益人群效应人群重叠,辅助化疗的益处不能彰显。
三、小结: ICAN研究显示,早期肺腺癌的EGFR基因突变状况与晚期相似。完全切除术后肺腺癌复发率和死亡率均较高。辅助化疗未提高生存。 综合ADUARA、CTONG1104(ADJUVANT)和ICAN研究的结果,我们可以初步得出以下结论,在EGFR敏感突变阳性完全切除术后IB-IIIA期肺腺癌中,与辅助化疗相比,辅助EGFR-TKI可改善DFS,不建议联合EGFR-TKI和化疗辅助治疗。I期肺腺癌,无论是否有EGFR基因敏感突变,均不推荐常规接受辅助化疗。 四、进一步的研究 ICAN研究是个前瞻性的非干预性研究,启动较早,未能检测更多驱动基因。随着近年来广谱分子检测的发展,完全切除术后的肺癌患者往往接受NGS检测,获得更多的驱动基因信息。刘思旸、吴一龙等利用ADJUVANT/CTONG1104中171个肿瘤组织进行基因组DNA提取和422个癌症相关基因的靶向NGS(二代测序),在EGFR突变背景下发现5个预测辅助治疗疗效的关键基因(TP53外显子4/5错义突变、RB1变异以及NKX2-1、CDK4和MYC扩增),并据此构建MINERVA评分模型(Multi-gene INdex to Evaluate the Relative benefit of Various Adjuvant therapies),完全切除EGFR突变型肺腺癌患者分为三种类型:优选TKI组(Highly TKI-Preferable group,HTP),倾向TIKI(TKI-Preferable group,TP)和倾向化疗组(Chemo-Preferable Group,CP)。据此类分子评分模型进行个体化决策,可能是进一步优选优势人群和治疗方案的未来重要方向。
参考文献
- WuYL, Tsuboi M, He J, et al; ADAURA Investigators. Osimertinib in resected EGFR-mutated non-small-cell lung cancer. N Engl J Med. 2020;383(18):1711-1723.doi:10.1056/NEJMoa2027071
- Yang, X.-N., et al. Real-World Survival Outcomes Based on EGFR Mutation Status in Chinese Patients With Lung Adenocarcinoma After Complete Resection: Results From the ICAN Study. JTO Clinical and Research Reports.2022
- Zhong WZ, Wang Q, Mao WM, et al. Gefitinib Versus Vinorelbine Plus Cisplatin as Adjuvant Treatment for Stage II-IIIA (N1-N2) EGFR-Mutant NSCLC: Final Overall Survival Analysis of CTONG1104 Phase III Trial. J Clin Oncol.2021;39(7):713-722.
- Liu SY, Bao H, Wang Q, et al. Genomic signatures define three subtypes of EGFR-mutant stage II-III non-small-cell lung cancer with distinct adjuvant therapy outcomes. Nat Commun. 2021;12(1):6450. Published 2021 Nov 8.
原文链接:http://www.xxwk.net/archives/621