以下文章来源于CardiothoracicSurgery ,作者CardiothoracicSurgery
摘 要
2021年WHO胸部肿瘤分类于今年早些时候发布,肺肿瘤分类是其中的章节之一。原则仍然是首先使用形态学,由免疫组织化学支持,然后是分子技术。2015年,特别强调使用免疫组织化学使分类更加准确。2021在整个书中更强调了所有肿瘤类型的分子病理学进展。本版的主要特点是:(1)比2015年世卫组织分类更广泛地强调基因检测;(2)专门用于小型诊断样本分类的部分;(3)继续建议记录浸润性非粘液性腺癌的组织学类型百分比,并利用这些特征应用正式的分级系统,根据第八版TNM分类推荐,在部分鳞状非粘液性肺腺癌中仅使用浸润性大小来确定T分级;(4)认识到通过空间传播是一种具有预后意义的组织学特征;(5)将淋巴上皮癌转移到鳞状细胞癌(分类);(6)肺神经内分泌肿瘤分类概念的更新;(7)确认细支气管腺瘤/纤毛粘液结节性乳头状瘤为腺瘤亚组中的新实体;(8)识别胸部SMARCA4缺陷未分化肿瘤;(9)纳入每个肿瘤的基本和理想诊断标准。
关键词:肺 癌症 病理 免疫组织化学 分子病理学 腺癌 鳞状细胞癌
引 文
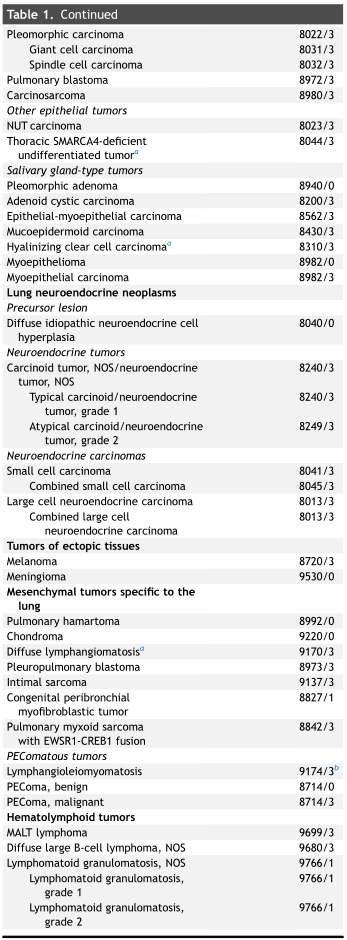
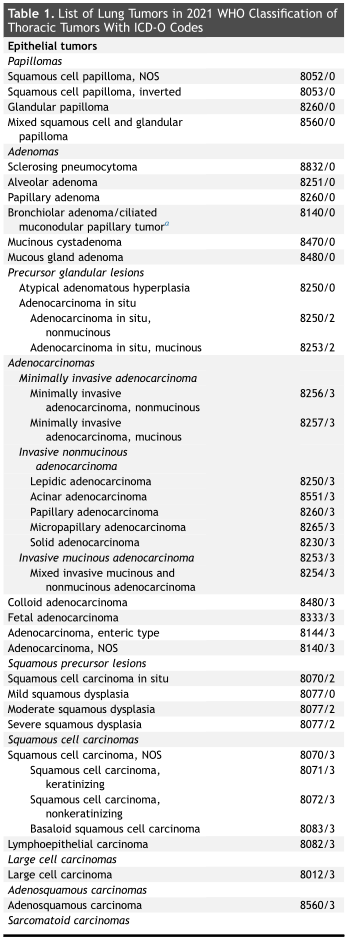
2021年世界卫生组织(WHO)胸部肿瘤分类于今年早些时候发布,肺肿瘤分类是其中的一章(表 1)。之前的WHO版本分别于1967年和1981年出版,单纯与肺有关,随后是 1999 年的肺和胸膜相关,然后是 2004 年和 2015 年的肺、胸膜、胸腺和心脏。2015 年的 WHO 分类书介绍了许多重要的巨大的变化,主要是由于在理解遗传学和分子靶向疗法方面取得了显著进展。由于在整个分类过程中引入了免疫组织化学和分子检测,许多更复杂的病理诊断方法已导致对肺肿瘤进行更精确的病理和遗传分类,从而提供更好的治疗策略。
肺肿瘤分类的原则仍然是首先使用形态学,由免疫组织化学支持,然后是分子技术。2015年,特别强调使用免疫组织化学使分类更加准确。2021 年,整本书更加强调所有肿瘤类型的分子病理学进展。个别分子异常构成了一些罕见肿瘤诊断标准的一部分,例如肺粘液样肉瘤伴EWSR1-CREB1 融合,但尽管许多分子异常尚未影响特定肿瘤亚型的分类,但它们可能会影响患者管理。
该版本的主要特点如下:(1)比2015年世卫组织分类更广泛地强调基因检测;(2)专门用于小型诊断样本分类的部分;(3)继续建议记录浸润性非粘液性腺癌的组织学类型百分比,并利用这些特征应用正式的分级系统,根据第八版TNM分类推荐,在部分鳞状非粘液性肺腺癌中仅使用浸润性大小来确定T分级;(4)认识到通过空间传播是一种具有预后意义的组织学特征;(5)将淋巴上皮癌转移到鳞状细胞癌(分类);(6)肺神经内分泌肿瘤分类概念的更新;(7)确认细支气管腺瘤/纤毛粘液结节性乳头状瘤为腺瘤亚组中的新实体;(8)识别胸部SMARCA4缺陷未分化肿瘤;(9)纳入每个肿瘤的基本和理想诊断标准。(补充表 1)。
更新的临床影响
美国的肺癌死亡率正在下降,2011 年国际肺癌研究协会 (IASLC)/美国胸科学会 (ATS)/欧洲呼吸学会 (ERS) 肺腺癌分类和 2015 年 WHO 分类中引入的主要变化通过更有效的分子和生物标志物测试提供更高的诊断准确性和更好的治疗策略,从而影响了这些患者预后的改善。美国癌症协会的早期数据显示,在美国,肺癌占过去 5 年癌症死亡人数整体下降的近一半,推动了 2017 年至 2018 年创下连续一年下降 2.5% 的历史第二。在 2013 年和 2018 年结束的两个 5 年期间,肺癌死亡率的年下降速度翻了一番多,从 2.4%下降到 5.5%。尽管许多因素促成了这些临床结果的改善,而且数据在国际上各不相同,但 2011 年 IASLC/ATS/ERS 腺癌分类和 2015 年 WHO 分类引入的基本原则通过准确诊断和促进分子和分子靶向和免疫疗法的生物标志物检测。
通过使用第 8 版非粘液性腺癌 TNM 分期分类也揭示了患者生存分层的改进,其中仅将侵入性大小用于 T 因子分级,这是基于使用 WHO 分类准确指定架构模式。关于手术治疗,对于小于或等于 2 cm 的小肺癌进行亚肺叶切除仍存在争议。最重要的是,应获得完整切除以获得最佳预后,因为非 R0 切除(包括所谓的不确定切除)的预期寿命会缩短。13将 STAS 识别为 WHO 分类中的组织学特征可能在该领域的未来发展中很重要。
关于系统治疗,在 2013 年至 2016 年间,NSCLC 死亡率的下降速度快于其发病率,而这种下降与生存率的显著改善相关,这与靶向治疗的批准时机相对应。这反映了 EGFR 和 ALK 抑制剂的临床应用对肿瘤具有特定基因组异常的患者的影响。此外,新发现的药物性基因驱动因子如 ROS1、RET、NTRK1-3、BRAF、MET 和 ERBB2 的影响,以及免疫疗法的影响和早期检测技术的实施,有望在未来几年进一步提高NSCLC的5年生存率。其中大部分仍取决于准确分类 NSCLC 亚型的能力,区分鳞状细胞癌和非鳞状非小细胞癌尤为重要,因此分子检测,包括程序性死亡配体 1 (PD-L1) 检测和尽管需要检测的肿瘤类型无疑会随着时间的推移而扩大,但对上述基因进行了适当的检测。事实上,随着更多潜在疗法的出现和分子病理学的进步,在选择最合适的治疗之前需要完整获取分子检测信息。这可能包括更多地考虑为什么免疫疗法治疗在某些患者中如此显著而在其他患者中根本没有,以及最初对治疗敏感的肿瘤如何获得耐药性,例如通过酪氨酸激酶抑制剂治疗后腺癌演变为小细胞癌。
相比之下,SCLC 的死亡率已与发病率下降相似的速度下降。一项研究表明,SCLC 死亡率的降低完全可以通过发病率的降低来解释,因为随着时间的推移,SCLC 患者的生存率没有改善。然而,在同一时期,对 SCLC 分子生物学的理解取得了重大进展,尽管形态学标准保持不变,但提出了新的分子分类,这有望成为对 SCLC 特定亚型开展新试验的驱动力,可能为有针对性的方法铺平道路,同样适用于 SCLC。
小型诊断样本
由于 70% 的肺癌处于晚期且无法切除,因此这些患者的诊断主要基于小活检和细胞学标本。因此,2011 年 IASLC/ATS/ERS 肺腺癌分类中引入了小样本肺癌的新分类,并在 2015 年 WHO 分类中采用。这些原发性或转移性肺肿瘤的小肿瘤样本是通过多种方法获得的,包括细针抽吸活检和剥落标本,例如痰液、支气管冲洗液和分泌物、支气管刷洗和支气管肺泡灌洗液。根据获取标本的当地医师(肺科医师、放射科医师、外科医生、细胞病理学家)的专业知识,最佳方法因机构而异。快速现场评估(包括远程病理学方法)有助于在手术时确认样本充分性,尽管这不是必需的。包括下一代测序在内的分子检测可以揭示细胞学样本的高诊断率,包括细胞块或乙醇固定涂片或液体制剂。获得多个活检样本,这些样本可以放入不同的石蜡块中,并分别用于免疫组织化学染色与分子检测是有帮助的。
这种管理小型活检和细胞学样本的工作流程强调了做出准确诊断的必要性,包括使用免疫组织化学等辅助技术对非小细胞癌 (NSCC) 进行特定组织学分型,并强调对分子检测的需求。为了节省尽可能多的组织用于分子检测,建议仅使用有限的免疫组化标记物和粘蛋白染色来诊断NSCC并确定其亚型。
推荐的良好临床实践指南(表 2)以及如何在小型活检中对肺癌进行分类的详细信息在其他出版物和表 3 和表 4 中进行了总结。记录小活检或细胞学标本中存在的腺癌模式可能会有所帮助,尽管与切除标本不同,不推荐记录模式的相对百分比。在某些临床情况下,例如立体定向放射治疗或热消融治疗,肺腺癌患者的核心活检中存在实性和/或微乳头状图案与不良预后相关。
在 TTF-1 和/或粘蛋白染色呈阳性但 p40 呈阴性的实性模式的低分化 NSCC 中,诊断为“NSCC,倾向于腺癌”(表 3)。在 TTF-1 和 p40 均为阴性的情况下,如果粘蛋白染色阳性,则可以支持腺癌的诊断。即使活检结果显示 TTF-1、p40 和粘蛋白染色呈阴性的实体 NSCC,也可以在细胞学标本上识别腺癌的特征以进行诊断。因此,活检和细胞学结果之间的相关性可能是有用的。事实上,低分化腺癌可以表现出明显的嗜酸性细胞质,提示角化(假鳞状细胞样外观),因此无法仅从形态上区分实性腺癌和鳞状细胞癌。最后,虽然 NSCC 缺乏分化的形态学证据需要免疫组织化学,但应尽量减少特殊染色的数量,以最大限度地增加可用于分子检测的组织。在大多数肿瘤中,仅对 TTF-1 和 p40 染色可以准确诊断腺癌或鳞状细胞癌(图 1A 和 B)。“NSCC 倾向于鳞状细胞癌”和“NSCC NOS”的诊断标准总结在表 3 中。NSCC-NOS 可能需要细胞角蛋白来确认癌和有限的免疫组织化学染色检查以排除转移。
某些小活检无法明确诊断,例如大细胞癌、多形性癌、腺鳞癌、原位腺癌 (AIS)、微创腺癌 (MIA) 和贴壁型为主的腺癌,因为这些需要切除标本。然而,表 4 中提供了活检提示其中一种实体时使用的术语。与过去相比,大细胞 NE 癌 (LCNEC) 的明确诊断通常可以在小活检中进行,因为更大的组织可用于进行检查。分子测试。这些较大的活检使识别清晰的 NE 形态和用诊断所需的 NE 免疫组织化学标记染色变得更容易。
用于预测性生物标志物测试的小活检样本
目前关于 NSCLC 治疗的国际指南建议对患者肿瘤样本进行常规检测,以检测 EGFR、ALK、ROS1、BRAF、V600E、NTRK1-3、RET、KRAS 和 MET 基因和 PD-L1 中是否存在驱动突变/融合免疫组化表达。在至少三分之二的晚期疾病患者中,检测是在诊断核心针或细胞学标本上进行的。对于分子检测,研究报告了对提交组织学或细胞学样本的活组织检查进行的 EGFR 检测的总体失败率、突变率或突变类型的可比结果,尽管肿瘤细胞性会影响检测成功或突变率,强调了分析前样品质量保证步骤,以确保最佳测试。
与应该存在于所有肿瘤细胞中的基因组驱动改变不同,PD-L1 蛋白表达在肿瘤内通常是异质的,并且它可能是动态的并且受先前治疗的影响。在 NSCLC 中,除了少数例外,只有肿瘤细胞上 PD-L1 的表达(肿瘤比例评分;表达膜染色的阳性细胞百分比)与免疫检查点抑制剂 (ICI) 治疗的预测生物标志物相关。试验数据显示,对保存或新鲜活检样本进行评估的 PD-L1 产生了可比较的临床结果。除了分析前问题外,样本充分性的最重要标准是存在至少 100 个可评估的肿瘤细胞以进行 PD-L1 评估。尽管作为预测 ICI 治疗临床益处的不完美标志物,PD-L1 检测目前仍然是一线 ICI 最可靠的预测标志物。
小活检和细胞学标本中肺癌诊断的病理学报告
针对基于小活检和细胞学的肺癌诊断报告提出了几项建议,包括以下内容:(1)根据 2021 年 WHO 分类进行病理或细胞病理学诊断;(2) 免疫组化和/或粘蛋白染色结果;(3) 对鉴别诊断的评论(适当时);(4) 是否有任何材料已提交进行分子检测的声明。指定使用哪个块以及应由外科病理学家或分子团队记录标本中活肿瘤细胞的百分比可能很有用。
腺癌
变更概览
自 2015 年以来,肺腺癌的分类基本保持不变,浸润性腺癌分为 MIA、浸润性非黏液性腺癌、浸润性黏液性腺癌 (IMA)、胶体腺癌、胎儿腺癌或肠型腺癌。这些区别于前体腺病变非典型腺瘤性增生或 AIS。侵袭性非粘液性腺癌是肺癌最常见的亚型,由具有腺分化的形态学或免疫组织化学证据的恶性上皮肿瘤组成,不符合任何其他类型腺癌的标准。腺体分化的形态学证据包括鳞屑状、腺泡状、乳头状或微乳头状生长模式。在纯实体瘤中,需要免疫组织化学(TTF-1 或 Napsin A)或组织化学(例如,D-PAS 染色显示 2 个高倍视野中的每个肿瘤细胞中有 5 个粘蛋白/w0.4 mm2)腺癌分化的证据用于诊断。对于非粘液性贴壁腺癌,为了分期,现在需要测量浸润(只有浸润成分的大小而不是总大小对T 分级有贡献),并且已经为浸润性肿瘤引入了分级系统(见随后的讨论和表 5)。应以 5% 至 10% 的增量记录每种组织学模式的百分比,以确定主要的组织学模式(亚型)并量化任何模式以确定肿瘤分级(见后续讨论)。对于侵袭的测量,除贴壁型(腺泡型、乳头状、微乳头状、实性或较少见的胶体型、肠型、胎儿型或 IMA)以外的任何组织学亚型或浸润肌纤维母细胞基质的肿瘤细胞灶都包括在肿瘤评估中,包括当侵入性组件不在一张幻灯片上的单个可测量焦点中时。
侵袭性非粘液性分级
腺癌
尽管目前对非粘液性腺癌的分类一直显示出与预后良好的相关性,但肺腺癌的正式分级系统一直缺乏。一般来说,贴壁型为主的肿瘤比腺泡或乳头状为主的腺癌预后更好,微乳头状和实体为主的肿瘤预后最差。“主要亚型”分类方案的预后价值的一个特殊缺点是“非主要”数量的不良预后模式,尤其是微乳头模式,即使仅包含肿瘤的一小部分,也与不良结果相关。因此,一直致力于开发一个正式的分级系统,以提供包含少量高级成分的更多预后信息,以及 IASLC 病理学委员会提出的侵袭性非粘液性腺癌的三层分级系统。这个提议的分级方案是基于主要组织学模式加上最差模式的组合,特别是考虑到高级模式:微乳头状、实性、筛状和复杂腺状模式,如果它们占肿瘤的至少 20%(图 2-4 和表 5)。这种提议的 IASLC 分级方案在大型验证队列中证明优于结合核或细胞分级、STAS 存在、坏死或其他负面预后特征的模型。
肿瘤STAS
STAS 被定义为主要肿瘤边缘以外空域内的肿瘤细胞(图 5)。以下特征有利于肿瘤细胞在 STAS 上的人为扩散:(1) 随机分布且边缘参差不齐的肿瘤细胞簇通常位于组织切片的边缘或组织切片平面之外;(2) 缺乏从肿瘤边缘到最远空域肿瘤细胞的空域连续扩散;(3) 具有良性细胞学特征和/或存在纤毛的肺细胞或支气管细胞;(4) 从肺泡壁升起的线性细胞条。使用这些标准,在对选定图像的研究中,STAS 与伪影的分离具有高度可重复性(平均 kappa 0.857)。STAS 的发生似乎不受总体标本处理程序的影响。腺癌中的 STAS 由三种形态学模式组成,包括微乳头结构、实心巢和不粘着的单细胞。STAS 与切除的肺腺癌的较差临床结果相关,并且所有研究的主要组织学肺癌类型。与接受肺叶切除术的患者相比,接受有限切除术的患者 STAS 与预后较差的关联似乎更强。由于 STAS 被视为肿瘤扩散的一种模式,因此它不包括在模式的总百分比或分期的肿瘤大小中。
IMA 和 AIS 和 MIA 的粘液性亚型
根据新的 WHO 分类,浸润性腺癌除了罕见的变异型外,还分为两大类,即非粘液型和粘液型。尽管临床实践中非粘液型更为常见,但粘液型仍占浸润性腺癌的 3% 至 10%。历史上,IMA 一词最早是在 IASLC/ATS/ERS 对腺癌的分类中提出的,以避免与粘液性细支气管肺泡癌混淆,后者的主要定义是非侵袭性肿瘤。事实上,虽然 IMA 可以显示鳞屑状生长模式,但侵入性模式始终存在。然而,许多但不是所有的 IMA 都以鳞屑病为主。在小于或等于 3 cm 且形态相似的小肿瘤中,可以诊断为 AIS 或 MIA 的粘液性亚型(如果浸润成分的大小 <5 mm)。IMA在组织学上被定义为由杯状细胞或柱状细胞形态组成的腺癌。免疫表型通常以 CK7+、TTF-1、CDX2 病灶、CK20 病灶和 HNF4a+ 为特征。由于编码 TTF-1 的基因 NKX2.1 的功能突变丧失,与胃肠道上皮细胞的分化重叠,被认为是可能的发病机制。在遗传上,这种肿瘤的特征是频繁的 KRAS 突变(62%–76%,主要是 G12D 和 G12V),其次是 NRG1 融合、ERBB2 改变(扩增和插入)和其他罕见的改变(ALK、ROS1、NTRK1、BRAF 的融合、RET、FGFR2/3 和 NRG2 以及 ERBB3 和 BRAF 的突变),以及低频率的 EGFR 和 TP53 突变,与侵袭性非粘液性腺癌相反。频繁的多灶性、多叶性和双侧表现是该肿瘤的另一个特征,最近发现这些病变之间存在克隆关系,提示 IMA 易发生肺内扩散。
腺癌的其他亚型
胶体型、胎儿型和肠型变体是罕见的亚型。胶体和肠型腺癌被认为与肺 IMA 具有相似的起源,因为其分子特征相同,大约一半的病例具有 KRAS 突变。如果与其他常规侵袭性非粘液性腺癌混合,超过 50% 的肿瘤显示细胞外粘蛋白池或肠形态是分别诊断胶体和肠腺癌的基本标准之一。与转移的区别通常通过临床手段进行,因为两种变体可能对肠道标志物(CDX2、CK20 和 Villin)呈阳性,而对肺细胞标志物(TTF-1 和 Napsin A)呈阴性或仅局灶性和弱阳性。
β-连环蛋白和 WNT 信号通路的异常在低级别或高分化胎儿腺癌的发病机制中至关重要,这使得它们在分子上不同于常规腺癌。高级别胎儿腺癌通常与其他类型的腺癌混合,诊断需要超过 50% 的高级别形态。较小的核异型性、桑椹的存在和核/细胞质 β-catenin 染色可区分低级别和高级别肿瘤。后者表现积极,预后不良。
腺癌的分子病理学
2015 年 WHO 分类(第四版)在“体细胞遗传学”部分报告了腺癌的分子异常。2021 年 WHO 分类将分子异常置于“病因”、“发病机制”和“诊断分子病理学”部分。现在已经报道了许多分子变化,这些变化与发病机制、进展以及重要的是与腺癌的治疗有关。
肺腺癌的分子特征鉴定了致癌驱动突变,其中一些是肺腺癌相对独特的(EGFR 外显子 19 缺失和外显子 21 点突变,EML4-ALK 易位)与几种相关的靶向治疗药物。匹配的已批准药物的靶向改变包括点突变、框内缺失、剪接变异和基因易位,例如 EGFR、ALK、BRAF、RET、NTRK1-3、ROS1 和 MET,以及 ERRB2 和 KRAS 中新兴的靶向性。尽管这些改变通常用于指导晚期患者的治疗,但 EGFR 靶向的使用已扩展到早期患者。仅在肺腺癌中发现的其他改变或与其他突变(包括 TP53、STK11 和 KEAP1)联合发现的其他改变目前不能直接靶向,但可能与肿瘤进展和对 STK11 的 ICI 抗性有关。在 2021 年 WHO 分类中,对肿瘤临床相关改变的评估被列为理想的标准,突出了其与分类层次结构的日益整合。
肺腺癌中这些改变的频率已按性别、年龄、吸烟状况和地理区域进行了研究。KRAS 突变,尤其是颠换型突变,在吸烟者中发现,而 EGFR 突变和 ALK、ROS1 和 RET 易位更可能在轻度或从不吸烟者中发现。TP53、NRAS 和 MAP2K1 等其他改变在吸烟者中也更常见;BRAF 和 MET 存在于吸烟者和非吸烟者中;EGFR 改变在年轻患者和女性中更常见,而 ALK、ROS1 和 RET 改变在年轻患者中更常见,但没有性别偏好。此外,显然 EGFR 突变在东亚更常见,而 KRAS 突变在美国/欧洲人群中更常见。其他变化也有不同的频率,而有些变化似乎在地理上没有变化(表 6)。众所周知,这些流行病学关联不是绝对的,因此不应决定检测。
尽管组织学亚型不应驱动分子检测的选择,但某些组织学模式更常与特定的改变相关。IMA 和以实体为主的腺癌通常是 KRAS 突变的肿瘤;在 IMA 中也发现了涉及 NRG1 的特定易位(参见前面的讨论)。高分化胎儿腺癌与 CTNNB1 突变有关。具有非粘液性鳞屑型和乳头状型的腺癌以及 TTF-1 阳性的腺癌更可能携带 EGFR 突变。发现 ALK 易位和 ROS1 和 RET 易位具有筛状/实心和印戒图案。
在未经治疗的环境中,致癌驱动因素通常在特定肿瘤中相互排斥。据推测,当相互排斥时,这些驱动因素是肿瘤形成的早期事件;这些改变存在于早期病变中,包括非典型腺瘤性增生和 AIS,支持了这一观点。此外,分子改变的这种相互排斥性可能为独立初选的分期提供支持性证据。
检测也与 ICI 的一线使用有关,因为 EGFR 突变的存在排除了这种情况。与 EGFR 突变一样,ALK 易位排除了 ICI 的一线治疗。尽管其他致癌改变可能与 ICI 反应降低有关,但它们不影响 ICI 一线治疗的决定。例如,STK11/LKB1 的改变也可能导致 PD-1 抑制剂耐药,但目前不排除它们的一线使用。
NE肿瘤:NE肿瘤分类框架
2021 年 WHO 分类将肺部 NEN 分类为一组肿瘤,分别包括低级别和中级别典型类癌 (TC) 和非典型类癌 (AC),以及高级别 NE 癌 (NEC),包括LCNEC 和 SCLC。然而,公认的是 TC 和 AC 在临床、流行病学、组织学、免疫组织化学和遗传学上与 LCNEC 和 SCLC 非常不同。NEC 与非 NEC 的结合以及“弥漫性特发性肺神经内分泌细胞增生”的实体也是本章的一部分。后者由病理学和临床标准定义:组织学上,它是与肿瘤和缩窄性细支气管炎相关的肺 NE 细胞的多灶性增生。它需要与继发于各种非肿瘤性疾病的局部反应性 NE 细胞增生区分开来。该分类对应于全身公认的通用框架,包括对应于类癌的分化良好的 NE 肿瘤 (NET) 和对应于 SCLC 和 LCNEC 的 NEC。然而,用于肺和胸腺的经典术语被保留,其中 TC 和 AC 通常对应于 NETs 1 级和 2 级的高分化类别,而低分化 LCNEC 和 SCLC 对应于 3 级 NEC。
当前的分类还保留了联合 LCNEC 和联合 SCLC 的类别,这可能占切除病例的 25%。这两种类型都包括 LCNEC 或 SCLC 与 NSCC 成分相结合,最常见的是腺癌或鳞状细胞癌。因此,显示 SCLC 和腺癌病灶的病例将被称为“联合 SCLC 和腺癌”。SCLC 也可以与 LCNEC 组合,并归类为“组合 SCLC 和 LCNEC”。在肺部,合并肿瘤通常发生在高级别癌而不是类癌中。这与消化和胰腺 NEN 不同,其中高级别和低级别肿瘤都可以包含外分泌腺成分,称为“混合神经内分泌/非神经内分泌肿瘤”。尽管 2021 年分类中的整体命名法基本没有变化,但有几个临床相关的更新。这些涉及活检、细胞学或转移性标本的术语、细胞增殖评估和特定标记的作用,以及遗传数据在 NEN 类别亚型中的潜在作用。
未特别指明的类癌和转移性类癌——标准和术语
肺 NEN 亚型的诊断标准仅基于形态学,有丝分裂和坏死是分类的主要依据。这些标准已在手术标本中得到验证,因为大多数 NEN 都进行了切除,但 SCLC 除外。然而,在小活检或细胞学标本中,准确的有丝分裂计数和坏死的识别通常很困难,因为有丝分裂计数可能是异质的。因此,建议使用术语“未特指类癌(NOS)”
对于来自原发性或转移性 NET 的小样本,并记录有丝分裂计数和任何坏死灶的存在(见随后讨论的标准),如果发现引起对 AC 的关注,请发表评论。尽管 Ki-67 增殖指数不是 2021 年 WHO 分类中的基本标准,但对于类癌肿瘤,它被作为一个理想的标准引入,将其纳入病理报告可能会有所帮助。这在评估转移性类癌标本时非常重要,以支持临床决策,因为医学肿瘤学家习惯于使用 Ki-67 指数对进展性消化和胰腺 NEN 的治疗选择进行分层。转移性肺(和胸腺)类癌采用类似方案治疗,在某些情况下可能需要 Ki-67 指数。在转移性类癌中,Ki-67 指数可能在极少数情况下超过标准标准,导致高级别 LCNEC 的鉴别诊断问题,并对治疗决策提出挑战。
评估增殖:有丝分裂计数和 Ki-67 的作用。
正如 2015 年 WHO 分类中已经详述的那样,仔细的有丝分裂计数至关重要,这是区分 TC 和 AC 以及区分类癌 (NET) 和高级 NEC 的最重要的形态学标准。当前的 WHO 版本建议在活动度最高的区域计算有丝分裂,并报告为每 2 平方毫米的图形数(不是 10 个高倍视野,以避免由于不同的显微镜模型而产生的差异)。此外,有人指出,在具有临界值的肿瘤中,接近预期的临界值,应计算三个 2平方毫米的区域并报告平均值;最后,只应计算明确的有丝分裂图,排除有问题的有丝分裂图,尤其是那些具有更多固缩细胞特征的细胞,例如细胞质嗜酸性粒细胞增多、存在核膜、核形状呈三角形或尖刺状。Ki-67 指数可用于从高级别肿瘤中分离类癌,包括具有广泛挤压伪影的活检中的 SCLC 和 LCNEC。尽管如此,考虑到在肺肿瘤中缺乏有效的评分规则,关于其预后有用性的文献相互矛盾,以及缺乏可重复的 TC 与 AC 和类癌的截止值,Ki-67 的作用并未被接受为 NEN 分类。与 LCNEC 和 SCLC 相比。
目前公布的数据报告平均 TC 的 Ki-67 值通常低于 5%,AC 的范围为 9% 至 18%,罕见的类癌病例超过这些值(见后续讨论)。Ki-67 指数超过 30% 通常表示高级 LCNEC 或 SCLC。
由于这些有争议的数据,肺(和胸腺)NEN 的诊断标准与其消化和胰腺 NEN 对应物的诊断标准仍然不同,其中 Ki-67 指数是 NET 和癌在三个等级中分层的诊断参数的组成部分。然而,目前的胸部肿瘤分类在理想的标准中提到了 Ki-67 指数的确定。然而,它在支持临床决策中的作用仍有待确定。
具有高增殖的类癌瘤。
近年来,有几篇论文报道了小系列的 NEN,其特征是类癌的分化良好的类器官形态,但有丝分裂每平方毫米计数超过 10 的增殖活性升高,因此符合诊断标准LCNEC 而不是类癌(图 6A)。这些病例的 Ki-67 指数也很高(图 6B),超过了通常在类癌中观察到的值(>20% 至 30%),特别是在它们的转移灶中,当那些可用于检测时。尽管在 1999 年的 WHO 分类中得到承认,但这些病例是如此罕见,在 20 年和随后的三个 WHO 分类之后,这些数据仅足以作为新出现的观察结果提及,而不是正式认可的实体。这些具有类癌形态的罕见肿瘤的确切分类仍然存在争议。它们对应于消化道和胰腺中称为 3 级 NET 的新实体,这些肿瘤似乎更常见。有证据表明,在肺中,它们与类癌的分子特征相同,而不是 LCNEC 或 SCLC。由于临床行为和对化疗的反应似乎与高级别 NEC 不同,因此识别这些罕见的 NEN 亚型具有临床意义。
目前的建议是将此类肿瘤标记为 LCNEC(基于高有丝分裂计数),然后添加说明类癌形态和 Ki-67 指数(如果有)的注释。在其他 NETs 的背景下,需要对这些肿瘤进行更多的研究,并提供仔细的病理学、临床和遗传数据。这是 IASLC 病理学委员会正在进行的调查领域。
结合 SCLC 和 LCNEC
这些可以“从头”发生或在腺癌中发生,其中 SCLC 发展为对特定疗法(如 EGFR 酪氨酸激酶抑制剂)耐药的表现。
伴有 NE 的非小细胞癌
差异化
在 10% 至 20% 的病例中,在缺乏任何 NE 形态的腺癌或鳞状细胞癌中,可以通过免疫组织化学检测 NE 分化。然而,这一发现没有任何临床影响,并且在没有 NE 形态的情况下,不建议在病理学实践中常规使用免疫组织化学。
新兴的遗传数据和概念
遗传和分子研究正在取得重大进展,特别是在高级小型和 LCNEC 方面。尽管当前的 WHO 分类没有引入肺部 NEN 的“分子分类”,但该书强调了可能为下一版提供信息的几个领域。其中包括:
- 尽管自 2015 年 WHO 分类以来肺的所有 NENs 都被纳入单一肿瘤谱系,但在类癌瘤 (NETs) 与高级别 LCNEC 和 SCLC 之间发现了主要的临床、流行病学、病理学和遗传差异(NEC)。
- 即使在每个单一 NEN 类别中,分子改变也存在差异,主要是中级 (AC) 和高级 (LCNEC 和 SCLC) 类型。高级别癌比类癌有更多的遗传改变,包括突变和扩增。
- 类癌的特征在于高达 40% 的病例中存在染色质重塑基因异常,并且在少部分病例中存在 MEN1、PSIP1 和 ARID1A 基因突变,而没有经典的 SCLC 基因改变(TP53/RB1 突变)。在比较基因组和转录组分析中,确定了几个分子簇,具有 LCNEC 形态的罕见肿瘤也可能包含类癌相关突变 (MEN1)。
- SCLC 始终与双等位基因 TP53 和 RB1 基因失活相关,但这并不意味着这种肿瘤类型在分子上是同质的。事实上,最近的转录数据揭示了肿瘤间的异质性,并确定了至少四种基因表达亚型,其中两种具有主要的 ASCL1 和 NEUROD1 基因改变,另外两种具有基因 POU2F3 和 YAP1 的异常。前两者与显著的 NE 分化相关,而后者尽管具有小细胞形态,但不表达 NE 标志物,而是至少部分对应于耐化疗的 SCLC 组。与这些亚型的临床相关性仍未完全确定,但最近的发现有助于更好地定义这些亚组。事实上,YAP1 亚型似乎不是一个单独的组,而是与其他三个重叠。相反,存在第四种 SCLC 亚型,定义为无 ASCL1、NeuroD1 和 POU2F3 突变(“三阴性”SCLC),具有明显的“炎症”特征,由免疫检查点分子和 T 淋巴细胞标志物的表达定义;这似乎与对 SCLC 化疗方案的耐药性有关。
- LCNEC 具有异质的分子特征,至少存在三个亚组,其中最小的包括 MEN1 突变病例,这些病例很可能代表具有高增殖率的类癌。其他两个亚组包括大多数 LCNEC,包括在 SCLC 中观察到的具有 TP53 和 RB1 基因突变的簇,以及在 NSCLC 中发生的具有 KRAS 和 STK11/KEAP1 突变的亚组。这种亚型可能具有相关的临床意义,因为 NSCLC 样类型对经典 SCLC 化疗方案可能有不同的反应。
鳞状细胞癌和 NUT 癌
对鳞状细胞癌的分类只做了一些小的调整。为了阻止其使用,不再推荐将“表皮样癌”作为相关术语。基底样癌仍然是肺鳞状细胞癌的一种亚型,但它与角化和非角化亚型并入同一章节。淋巴上皮样癌,在第四版中属于“其他和未分类的癌”,现在更名为淋巴上皮癌,归类为 CK5/6、p40、p63 弥漫性阳性染色的鳞状细胞癌,不同合胞体生长模式、可变的淋巴浆细胞浸润以及与 Epstein-Barr 病毒的频繁关联(图 7A)。通过原位杂交证明 EBER1 的存在被认为是理想的诊断标准,因为 EBV 阴性淋巴上皮癌会发生,特别是在欧洲血统的患者中。相比之下,在亚洲患者中超过 90% 的病例中发现 EBER1 阳性染色(图 7B)。
与肺腺癌不同,肺鳞状细胞癌的分子特征尚未有重大发现。对于鳞状细胞癌患者来说,治疗上可靶向的驱动突变仍然难以捉摸,但他们可能会受益于单独或联合化疗的抗程序性细胞死亡蛋白-1/PD-L1 治疗。然而,EGFR 和 MET 突变,以及 ALK 或 ROS1 重排,可能发生在肺鳞状细胞癌中,尤其是在年轻的从不吸烟的鳞状细胞癌患者中;因此,在这个临床组中,对这些驱动突变进行分子检测是必不可少的。
NUT 癌是另一种肿瘤,尽管并非总是如此,但通常具有鳞状细胞分化和 P40 阳性。虽然它可能原发于肺,但在胸腺肿瘤中作为胸腺 NUT 癌进行了讨论。对于通常具有小细胞形态并可能揭示鳞状细胞形态证据的恶性肺肿瘤患者,应考虑直接或间接检测 NUTM1 基因重排的相关研究,包括免疫组织化学,特别是当临床特征不典型为鳞状细胞时癌(年轻,轻度或从不吸烟史)(图 8A 和 B)。
BA/CMPT及其鉴别诊断
定义和主要组织学特征
BA/CMPT 是 2021 年 WHO 分类中的一个新实体,被认为是一种肺腺瘤。BA/CMPT 最初是在 CMPT 的名称下描述的。最近,有人提出 CMPT 代表了具有更广泛形态学谱的病变中突出的粘液/乳头状形态,概括了细支气管分化,因此促使 BA 的总称涵盖具有经典形态或 CMPT 的病变家族以及那些缺乏显著的粘液性、乳头状和纤毛特征。BA/CMPT 的定义特征包括沿着平淡的双层细支气管型上皮的肺泡实质的结节性增殖,包含围绕管腔细胞的连续基底细胞层。管腔细胞的分化范围可以从类似于近端气道的那些,因此含有丰富的纤毛和/或粘液细胞(图 9A 和 B),以及那些类似于远端气道,因此主要含有立方形的 TTF-1 阳性细胞,具有只有纤毛和粘液细胞很少或缺失(图 9C 和 D)。尽管近端型病变往往呈明显的乳头状,但远端型病变往往是完全扁平的或仅局部呈乳头状。外周和近端 BA/CMPT 的区别只是为了帮助识别它们的形态谱,但这种区别并不是诊断所必需的,特别是考虑到一些病变在近端谱中具有混合的组织学特征——远端分化。
BA/CMPT 的另一个常见形态特征是存在含有纤毛细胞的微乳头簇。此外,这些病变可以沿肺泡壁有限的不连续扩散,与 IMA 中发现的跳跃病变非常相似。可能存在中央瘢痕和弹性纤维断裂。这些发现不应被视为恶性肿瘤的特征。
虽然通常可以通过苏木精和伊红诊断 BA/CMPT,但免疫组织化学可能会有所帮助,尤其是在核心活检中。基底细胞标记(p63/p40 或 CK5/6)通过突出连续基底层的存在是关键的诊断辅助(图 9E)。
分子特征
在分子上,BA/CMPT 表现出高度独特的轮廓,其特征在于单个驱动器更改,最常见的是涉及 BRAF V600E(图 9F)。其他报道的改变包括非典型 EGFR 外显子 19 缺失、EGFR 外显子 20 插入,以及涉及 KRAS、HRAS、ALK 和 AKT1 的改变。远端和近端 BA 的分子变化谱总体相似(后者对应于经典 CMPT),支持它们的疾病学关系。
临床表现
临床上,BA/CMPT 表现为偶发性病变,计算机断层扫描检测为周围肺结节,可为实性或毛玻璃状,部分有空洞。病变通常很小,通常为 0.5 至 1.5 厘米。患者为中老年,中位年龄72岁,无性别倾向。迄今为止报告的所有 BA/CMPT 患者在手术切除后均未患病。
鉴别诊断
鉴于它们的良性性质,BA/CMPT 最重要的鉴别诊断考虑因素是腺癌。特别是近端型 BA/CMPT,具有突出的粘液特征和外周跳跃性病变,鉴别诊断包括 IMA。几项研究强调了在术中会诊期间区分 CMPT/BA 与腺癌,尤其是 IMA 的挑战,因为纤毛和基底细胞的存在在冰冻切片中可能很细微。
近端型 BA/CMPT 在形态上与腺性/混合性乳头状瘤无法区分,除了前者位于肺泡肺实质而后者位于支气管内。有人提出 BA/CMPT 与支气管乳头状瘤之间存在潜在的疾病关系,但需要进一步研究。外周 BA/CMPT 与细支气管周围化生的区别在于它们表现为离散的结节。
SMARCA4缺陷未分化胸腔肿瘤
第五版中新增的实体是一种高级恶性肿瘤,具有未分化或横纹肌样表型和缺乏 SMARCA4(也称为 BRG1),这是 BAF (SWI/SNF) 染色质重塑复合物的关键成员。这种疾病以前被称为“SMARCA4缺陷型胸部肉瘤”。然而,最近的分子证据表明其与吸烟相关的 NSCLC 具有密切的基因组关系,因此大多数例子越来越多地被重新解释为去分化/未分化肺癌。这导致决定将该实体重新命名并置于“肺部其他上皮肿瘤”类别下,但对少数病例可能存在替代致病途径有所保留。尽管如此,WHO 分类将胸部 SMARCA4 缺陷未分化肿瘤 (SMARCA4-UT) 识别为与具有 SMARCA4 缺陷的传统 NSCLC 不同的实体,因为其具有不同的表型。
胸部 SMARCA4-UT 通常影响具有显著男性偏好和大量吸烟史的中青年。肿瘤表现为纵隔、肺门、肺和/或胸膜中的一个大的压迫性肿块,与转移有关。由于具有相似表型的肿瘤可能出现在其他地方(例如腹部)并转移到胸部,因此临床相关性是强制性的。胸部 SMARCA4-UT 是一种高度侵袭性肿瘤,中位总生存期为 4 至 7 个月。它们通常对细胞毒性化学疗法无反应。
组织学由散布的片状不连贯的、大的、圆形的上皮样细胞组成,具有泡状染色质和突出的核仁。细胞核相对单调,偶尔有细胞表现出轻度的多形性。可能存在横纹肌样细胞,但它们不是诊断所必需的。整体形态学谱让人想起在小儿恶性横纹肌瘤中发现的形态学谱。应不存在明确的上皮结构(例如,腺体或鳞状细胞分化),但罕见的合并常规 NSCLC 的病例除外。SMARCA4 (BRG1) 免疫组化表达丢失或严重降低。SMARCA2 (BRM) 染色在大多数情况下会丢失,其中许多会表达 CD34、SOX2 和/或 SALL4。细胞角蛋白常表现为局灶/弱表达,可能完全阴性,claudin-4阴性或仅局灶阳性(图10A和B)。
肿瘤是由 SMARCA4 的双等位基因失活驱动的,但如果免疫组织化学证实 SMARCA4 缺乏,则不需要测序来诊断。高达 44% 的病例在 KRAS、STK11 和/或 KEAP1 中有额外的突变,这些突变是吸烟相关 NSCLC 的常见驱动因素。大多数肿瘤还具有基因组吸烟突变特征和高肿瘤突变负担,类似于非小细胞肺癌。然而,胸部 SMARCA4-UT 的转录谱不同于 SMARCA4 缺陷的常规 NSCLC,但与恶性横纹肌瘤相似。
大约 5% 的常规 NSCLC 缺乏 SMARCA4;然而,胸部 SMARCA4-UT 被认为是与 SMARCA4 缺陷型 NSCLC 不同的实体,因为它具有显著的组织学、免疫组化、临床和预后差异。与传统的 NSCLC 不同,SMARCA4-UT 缺乏上皮结构(例如腺体)和弥漫性强角蛋白表达。辅助标志物(SMARCA2、claudin-4、CD34、SALL4 和 SOX2)也有助于区分,尽管这些标志物都不是完全敏感或特异的。重要的是,常规 SMARCA4 染色不推荐用于常规 NSCLC,但仅适用于怀疑 SMARCA4-UT 的情况。
其他肿瘤
透明细胞癌
在本版分类中,透明细胞癌已被添加到唾液腺型肿瘤组中。虽然很少见,但这在气道中得到了充分的描述,值得纳入。这些肿瘤具有 EWSR1-ATF1 基因融合,本书保留了“透明化透明细胞癌”这一术语,而 WHO 头颈部肿瘤分类已将名称改为透明细胞癌,因为保持这两者之间的区别很重要具有清晰细胞形态的肿瘤和非小细胞肺癌。
黑色素瘤和脑膜瘤
在 2015 年 WHO 分类中,创建了一个名为“异位起源的肿瘤”的组,以涵盖更常见于其他部位但极少数表现为原发性肺肿瘤的肿瘤,可能来自异位组织巢。这些是黑色素瘤、胸腺瘤和脑膜瘤。任何在肺活检中被归类为上述肿瘤之一的样本都需要对更常见部位的隐匿性原发灶进行深入的临床审查,然后再将其指定为原发性肺肿瘤,即使在细胞学外观良性的情况下(例如,良性转移性脑膜瘤) ),但对罕见的原发病例进行了很好的描述。在 2021 年 WHO 分类中,该类别仍然存在,尽管胸腺瘤在单独的章节中进行了讨论。此外,对于黑色素瘤,最近的数据表明,即使在其他地方没有可识别的原发性,据称肺黑色素瘤仍然具有阳光损伤的突变特征。这表明它们可能是由退化的原发性皮肤肿瘤转移的,尽管某些黑色素瘤可能来自肺气道的可能性并未完全排除。
炎性肌纤维母细胞瘤
尽管表 1 总结了 10 种特定于肺的间充质肿瘤,但遗传进展最多的间充质肿瘤是炎症性肌纤维母细胞瘤(IMT),它被放置在“胸部间充质肿瘤”一章中。与肺外部位相比,融合可以在高比例的肺 IMT 中找到。ALK 重排是最常见的,其中大多数可以通过免疫组织化学与 D5F3 或 5A4 抗体检测到。如果免疫组织化学对 ALK 呈阴性,则通过免疫组织化学(使用 ROS1 或泛 NTRK 抗体)和其他分子检测(如荧光原位杂交、多重 RNA 测序或 NanoString 检测)进一步寻找融合可能有助于检测几乎所有肺 IMT 中的融合。
未来的工作
本综述强调,尽管大多数肿瘤的形态学定义变化相对较小,但内在细节显著增加,特别是与分子进展相关的细节。这些数据是确定未来工作方向的模板,可能会在准确性、可重复性和与患者管理的相关性方面改进分类。示例包括 (1) 验证提议的 IASLC 切除腺癌分级系统,并在小活检中对切除的鳞状细胞癌和 NSCLC 进行分级;(2) 通过进一步研究具有高有丝分裂或增殖率的 AC,改进 NEN 的分类;(3) 更好地了解 SCLC 和 LCNEC 的形态学和遗传谱的临床意义;(4) 扩大诊断分子检测对更多肿瘤类型的作用。
翻译及审校:张其鹏 王琳瑶
原文链接:http://www.xxwk.net/archives/452